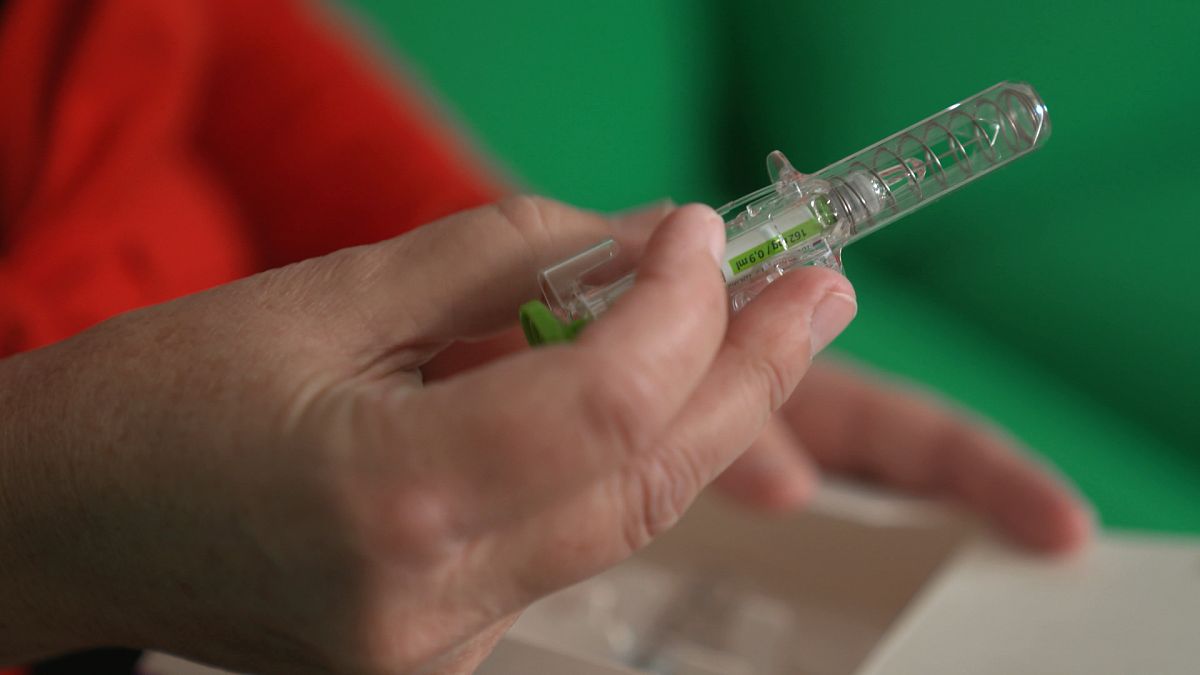
Los biosimilares son medicamentos biológicos cuya estructura, eficacia, seguridad, dosificación y efectos secundarios son muy similares a los de los medicamentos de referencia aprobados. Pero son más baratos de fabricar y más asequibles para los pacientes y los sistemas sanitarios.
Connie Ziegler dice que no recuerda realmente cuándo empezaron sus problemas de salud.
"Cuando tenía un año y medio, mis padres me dijeron que me empezaban a doler especialmente las rodillas. Y que no quería caminar mucho. Y empecé a tener dolores. No mucho después de eso y de los primeros síntomas, me diagnosticaron artritis reumatoide juvenil", cuenta a Euronews.
Connie, que ahora tiene 54 años, trabaja como gestora de proyectos en la Asociación Danesa de Reumatismo, en Copenhague.
Empezó a tratarse a los 20 años, y hace unos diez años, los médicos le aconsejaron cambiar su medicación habitual por biosimilares.
¿Qué son los biosimilares?
Los biosimilares son medicamentos biológicos cuya estructura, eficacia, seguridad, dosificación y efectos secundarios son muy similares a los de los medicamentos de referencia aprobados.
Pero son más baratos de fabricar y más asequibles para los pacientes y los sistemas sanitarios. Dinamarca ha sido pionera en su uso. El país también tiene una buena tradición en el seguimiento de sus pacientes.
Como Connie, miles de pacientes daneses se han pasado con éxito a los biosimilares estos últimos años.
Tan pronto como los biosimilares estuvieron disponibles, los expertos empezaron a estudiar su impacto. Bente Glintborg, consultora principal de Reumatología, participó en varios de esos estudios:
"Identificamos a más de 1000 pacientes que habían cambiado y a un grupo histórico de pacientes tratados con el fármaco original el año anterior. Y así podemos comparar. Y los resultados fueron muy idénticos. Apenas podíamos separar las líneas. Esto nos demostró que los pacientes aceptaron el cambio a los medicamentos biosimilares y obtuvieron los mismos resultados que con el fármaco original".
Mejorar el acceso a biosimilares en la UE
Reconociendo estos avances, la reforma farmacéutica de la Comisión Europea quiere mejorar la disponibilidad de biosimilares -y también de genéricos- para garantizar que más pacientes tengan acceso a medicamentos más asequibles.
Los incentivos modulados deberían permitir que los biosimilares entren en los mercados hasta 2 años antes que en la actualidad, afirma la Comisión.
Desde los Países Bajos, la Agencia Europea de Medicamentos (EMA) seguirá desempeñando un papel clave a nivel consultivo y regulador.
La Agencia autorizó el primer biosimilar en 2006. Desde entonces, se han aprobado 105 en la Unión Europea. Otros candidatos están bajo estricta vigilancia, dice el director médico de la EMA, Steffen Thirstrup:
"Lo que buscamos aquí dentro es asegurarnos de que el fabricante puede producir estos productos de forma consistente y segura. Que lo que producen es lo que prometieron producir y que han demostrado que el producto, desde el punto de vista molecular, es similar al producto de referencia", dice Thirstrup.
Mientras que algunos críticos tendrían dudas, y argumentarían que los biosimilares tienen los estándares son más bajos, el dr. Thirstrup dice que esto no es verdad. Los estándares son los mismos independientemente del tipo de medicamento que está siendo tratado.
"Cuando se introdujeron los genéricos hace 30 o 40 años, teníamos las mismas preocupaciones. Sigue habiendo rumores de vez en cuando de que los genéricos, por ser más baratos, ofrecen menos calidad. Y eso no es cierto", señala Thirstrup.