Investigadores del CNB-CSIC han logrado que la bacteria Pseudomonas putida consuma dinitrotolueno (DNT), un residuo tóxico del TNT, como única fuente de energía. El proceso abre vías para descontaminar suelos en zonas de conflicto bélico.
El Centro Nacional de Biotecnología del CSIC acaba de publicar en la revista 'Metabolic Engineering' un resultado que varios equipos internacionales habían intentado obtener sin éxito durante años: conseguir que una bacteria no solo tolere el 2,4-dinitrotolueno (DNT), sino que lo use como alimento.
 PUBLICIDAD
PUBLICIDAD
 PUBLICIDAD
PUBLICIDAD
El DNT es un compuesto sintético estrechamente ligado a la producción del trinitrotolueno, más conocido como TNT. No aparece en la naturaleza por sí solo; es producto de la industria armamentística y persiste en los suelos contaminados por conflictos bélicos durante décadas, acumulándose en el terreno sin que los ecosistemas tengan mecanismos eficaces para eliminarlo.
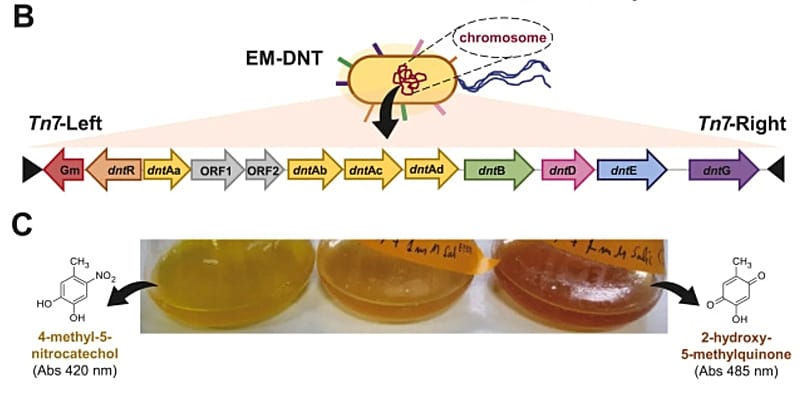
La bacteria elegida para el experimento fue 'Pseudomonas putida', un microorganismo conocido en microbiología por su capacidad para sobrevivir en ambientes hostiles. El equipo, liderado por el investigador Víctor de Lorenzo, partió de una modificación genética previa que dotaba a la bacteria de los genes necesarios para degradar el DNT. El problema era que tenerlos no era suficiente: la bacteria no lograba crecer en presencia del compuesto.
La estrategia ha sido obligarla a adaptarse o morir
El método que resolvió el problema fue, en cierto sentido, brutal en su sencillez. El equipo sometió a la bacteria a dosis subletales de DNT de forma progresiva, en un entorno donde los nutrientes convencionales iban desapareciendo. La idea era forzar mutaciones que no solo permitieran sobrevivir en ese entorno, sino que convirtieran el compuesto tóxico en la única fuente posible de carbono y nitrógeno.
"Al cabo de un año de cultivo, hemos conseguido que la bacteria asimile el DNT como única fuente nutritiva", explicó David Rodríguez-Espeso, investigador del CNB-CSIC y uno de los autores del estudio. Los productos finales del proceso son biomasa celular, dióxido de carbono y agua, lo que implica la eliminación completa del compuesto y de los intermediarios tóxicos que se generan durante su degradación.
El análisis genético posterior reveló cambios en más de 50 genes, relacionados con la respuesta al estrés químico y los mecanismos de reparación del ADN. Esos ajustes fueron los que permitieron a la bacteria tolerar los derivados tóxicos que aparecen antes de que el DNT sea completamente degradado, que era precisamente el punto donde los intentos anteriores habían fracasado.
Por qué fallaron los estudios previos
Antes de este trabajo, la investigación sobre degradación bacteriana de DNT había identificado el sistema genético de bacterias del género Burkholderia capaces de crecer en suelos contaminados con este compuesto. Sin embargo, nadie había logrado replicar ese comportamiento en otro organismo con la eficacia suficiente para plantear una aplicación real.
"No habían podido encontrar una bacteria que utilizara el DNT como fuente única de carbono y nitrógeno", señaló De Lorenzo. La clave, según los autores, estaba en que el proceso requería una metodología lenta, que no producía resultados a corto plazo. Los enfoques anteriores buscaban atajos que el problema no permitía.
El resultado publicado ahora responde a esa pregunta: la bacteria necesitaba ajustes genéticos que no podían introducirse de golpe mediante ingeniería genética convencional, sino que debían emerger a través de una evolución adaptativa guiada en el laboratorio.
Descontaminar lo que dejó la guerra
Los suelos contaminados por residuos de explosivos son uno de los problemas medioambientales más persistentes en zonas de postconflicto. El DNT y otros compuestos relacionados se acumulan en el terreno alrededor de polígonos militares, fábricas de armamento abandonadas y campos de batalla, con consecuencias tóxicas para los ecosistemas locales y para las personas que viven cerca.
Las soluciones actuales de descontaminación son en su mayoría físicas o químicas, costosas y difíciles de aplicar a gran escala. La biología sintética lleva años explorando alternativas microbianas, pero los avances concretos han sido escasos.
Este trabajo, desarrollado íntegramente en condiciones de laboratorio, no es todavía una solución lista para su despliegue en campo. Los investigadores son cautelosos al respecto. Pero demuestra que es posible diseñar microorganismos capaces de completar la degradación de un compuesto que la naturaleza, por sí sola, apenas puede procesar.